Существует 2 теории растворов : физическая и химическая .
Физическая теория растворов.
Была открыта Якобом Г. Вант-Гоффом и Свате А.Аррениусом.
Суть теории растворов : растворитель - химическая индифферентная среда, в которой равномерно распределены частицы растворенного вещества. Теория не предполагает наличие межмолекулярных связей между растворителем и растворенным веществом.
Под эту теорию подходят только идеальные растворы, где компоненты растворителя никак не воздействуют на растворимое соединение. Примером являются газовые растворы, где нереагирующие между собой газы смешиваются друг с другом в неограниченных количествах. Все физические данные (температура кипения и плавления, давление, теплоемкость) вычисляется исходя из свойств всех соединений, входящих в состав.
По закону Дальтона : общее давление газовой смеси равно сумме парциальных давлений ее компонентов:
P общ = Р 1 + Р 2 + Р 3 +…
Химическая теория растворов.
Химическую (сольватную) теорию растворов описал Д.И. Менделеев . Суть заключается в следующем: частицы растворителя и растворенного вещества реагируют друг с другом, в результате чего получаются нестойкие соединения переменного состава - гидраты (сольваты ). Основные связи тут - водородные.
Вещество может распадаться на слои (растворяться) в случае полярного растворителя (воды). Ярким примером является растворение поваренной соли.
Также может проткать реакция между компонентами смеси:
H 2 O +Cl 2 = HCl + HOCl ,
В ходе процесса растворения происходит изменение состава и объема реакционной смеси, т.к. протекают 2 процесса: разрушение структуры растворяемого вещества и химическая реакция между частицами. Оба процесса идут с изменением энергии.
Тепловые эффекты могут быть экзотермическими и эндотермическими (с выделением и поглощением энергии).
Соединения с частицами растворителя называются гидратами .
Кристаллические вещества, в состав которых входят гидраты, называются кристаллогидратами и имеют различную окраску. Например, кристаллогидрат сульфата меди: CuSO 4 ·5 H 2 О . Раствор кристаллогидрата синий. Если рассмотреть кристаллогидрат кобальта CoCl 2 · 6 H 2 O , то он обладает розовым цветом, CoCl 2 · 4 H 2 O - красный, CoCl 2 ·2 H 2 O - сине-фиолетовый, CoCl 2 · H 2 О - темно-синий, а безводный раствор хлорида кобальта - бледно-синего цвета.
РАСТВОРЫ
Растворы - компонентами.
«растворитель» и «растворенное вещество» полярные неполярные
гидрофильные (притягивающие воду) и гидрофобные дифильными
Теории растворов
Физическая теория растворов.
идеальными
Химическая теория растворов.
Химическая, или сольватная, теория растворов была предложена в 1887 г. Д.И. Менделеевым, который установил, что в реальном растворе присутствуют не только индивидуальные компоненты, но и продукты их взаимодействия. Исследования водных растворов серной кислоты и этилового спирта, проведенные Д.И. Менделеевым, легли в основу теории, суть которой заключается в том, что между частицами растворенного вещества и молекулами растворителя происходят взаимодействия, в результате которых образуются нестойкие соединения переменного состава, называемые сольватами или гидратами , если растворителем является вода. Главную роль в образовании сольватов играют непрочные межмолекулярные силы, в частности, водородная связь.
В этой связи следует принять следующую трактовку понятия «раствор»:
Раствором называется гомогенная система переменного состава, состоящая из двух и более компонентов и продуктов их взаимодействия.
Из данного определения следует, что растворы занимают промежуточное положение между химическими соединениями и смесями. С одной стороны, растворы однородны, что позволяет рассматривать их как химические соединения. С другой стороны, в растворах нет строгого стехиометрического соотношения между компонентами. Кроме того, растворы можно разделить на составные части (например, при упаривании раствора NaCl можно выделить соль в индивидуальном виде).
Связь между различными способами
Кислоты и основания
Несмотря на то, что понятия «кислота» и «основание» широко используются для описания химических процессов, единого подхода к классификации веществ с точки зрения отнесения их к кислотам или основаниям нет. Существующие в настоящее время теории (ионная теория С. Аррениуса , протолитическая теория И. Бренстеда и Т. Лоури и электронная теория Г. Льюиса ) имеют определенные ограничения и, таким образом, применимы лишь в частных случаях. Остановимся подробнее на каждой из этих теорий.
Теория Аррениуса.
В ионной теории Аррениуса понятия «кислота» и «основание» тесно связаны с процессом электролитической диссоциации:
Кислотой является электролит, диссоциирующий в растворах с образованием ионов Н + ;
Основаниемявляется электролит, диссоциирующий в растворах с образованием ионовОН - ;
Амфолитом (амфотерным электролитом) является электролит, диссоциирующий в растворах с образованием как ионовН + , так и ионов ОН - .
Например:
НА ⇄ Н + + А - nH + +MeO n n - ⇄Ме(ОН) n ⇄Ме n + +nОН -В соответствии с ионной теорией кислотами могут быть как нейтральные молекулы, так и ионы, например:
HF ⇄ H + + F -
H 2 PO 4 - ⇄ H + + HPO 4 2 -
NH 4 + ⇄H + +NH 3
Аналогичные примеры можно привести и для оснований:
КОН К + + ОН -
- ⇄Al(OH) 3 + ОН -
+ ⇄Fe 2+ + ОН -
К амфолитам относят гидроксиды цинка, алюминия, хрома и некоторые другие, а также аминокислоты, белки, нуклеиновые кислоты.
В целом, кислотно-основное взаимодействие в растворе сводится к реакции нейтрализации:
H + + ОН - H 2 O
Однако, ряд экспериментальных данных показывает ограниченность ионной теории. Так, аммиак, органические амины, оксиды металлов типа Na 2 O, СаО, анионы слабых кислот и т.д. в отсутствии воды проявляют свойства типичных оснований, хотя не имеют в своем составе гидроксид-ионов.
С другой стороны, многие оксиды (SO 2 , SO 3 , Р 2 О 5 и т.д.), галогениды, галогенангидриды кислот, не имея в своем составе ионов водорода, даже в отсутствии воды проявляют кислотные свойства, т.е. нейтрализуют основания.
Кроме того, поведение электролита в водном растворе и в неводной среде может быть противоположным.
Так, CH 3 COOH в воде является слабой кислотой:
CH 3 COOH⇄CH 3 COO - +H + ,
а в жидком фтороводороде проявляет свойства основания:
HF + CH 3 COOH⇄CH 3 COOH 2 + +F -
Исследования подобных типов реакций и в особенности реакций, протекающих в неводных растворителях, привели к созданию более общих теорий кислот и оснований.
Теория Бренстеда и Лоури.
Дальнейшим развитием теории кислот и оснований явилась предложенная И. Бренстедом и Т. Лоурипротолитическая (протонная) теория. В соответствии с этой теорией:
Кислотой называют любое вещество, молекулы (или ионы) которого способны отдавать протон, т.е. быть донором протона;
Основанием называют любое вещество, молекулы (или ионы) которого способны присоединять протон, т.е. быть акцептором протона;
Таким образом, понятие основания значительно расширяется, что подтверждается следующими реакциями:
ОН - + Н + Н 2 О
NH 3 +H + NH 4 +
H 2 N-NH 3 + +H + H 3 N + -NH 3 +
По теории И. Бренстеда и Т. Лоури кислота и основание составляют сопряженную пару и связаны равновесием:
КИСЛОТА ⇄ ПРОТОН + ОСНОВАНИЕ
Поскольку реакция переноса протона (протолитическая реакция) обратима, причем в обратном процессе тоже передается протон, то продукты реакции являются друг по отношению к другу кислотой и основанием. Это можно записать в виде равновесного процесса:
НА + В ⇄ ВН + + А - ,
где НА – кислота, В – основание, ВН + – кислота, сопряженная с основанием В, А - – основание, сопряженное с кислотой НА.
Примеры.
1) в реакции:
HCl+OH - ⇄Cl - +H 2 O,
HCl и H 2 O – кислоты, Cl - и OH - – соответствующие сопряженные с ними основания;
2) в реакции:
HSO 4 - +H 2 O⇄SO 4 2 - +H 3 O + ,
HSO 4 - и H 3 O + – кислоты, SO 4 2 - и H 2 O – основания;
3) в реакции:
NH 4 + +NH 2 - ⇄ 2NH 3 ,
NH 4 + – кислота, NH 2 - – основание, а NH 3 выступает в роли как кислоты (одна молекула), так и основания (другая молекула), т.е. демонстрирует признаки амфотерности – способности проявлять свойства кислоты и основания.
Такой способностью обладает и вода:
2Н 2 О ⇄ Н 3 О + + ОН -
Здесь одна молекула Н 2 О присоединяет протон (основание), образуя сопряженную кислоту – ион гидроксония Н 3 О + , другая отдает протон (кислота), образуя сопряженное основание ОН - . Этот процесс называется автопротолизом .
Из приведенных примеров видно, что в отличие от представлений Аррениуса, в теории Бренстеда и Лоури реакции кислот с основаниями не приводят к взаимной нейтрализации, а сопровождаются образованием новых кислот и оснований.
Необходимо также отметить, что протолитическая теория рассматривает понятия «кислота» и «основание» не как свойство, но как функцию, которую выполняет рассматриваемое соединение в протолитической реакции. Одно и то же соединение может в одних условиях реагировать как кислота, в других – как основание. Так, в водном растворе СН 3 СООН проявляет свойства кислоты, а в 100%-й H 2 SO 4 – основания.
Однако, несмотря на свои достоинства, протолитическая теория, как и теория Аррениуса, не применима к веществам, не содержащим атомов водорода, но, в тоже время, проявляющим функцию кислоты: галогенидам бора, алюминия, кремния, олова.
Теория Льюиса.
Иным подходом к классификации веществ с точки зрения отнесения их к кислотам и основаниям явилась электронная теория Льюиса. В рамках электронной теории:
кислотой называют частицу (молекулу или ион), способную присоединять электронную пару (акцептор электронов);
основанием называют частицу (молекулу или ион), способную отдавать электронную пару (донор электронов).
Согласно представлениям Льюиса, кислота и основание взаимодействуют друг с другом с образованием донорно-акцепторной связи. В результате присоединения пары электронов у атома с электронным дефицитом возникает завершенная электронная конфигурация - октет электронов. Например:

Аналогичным образом можно представить и реакцию между нейтральными молекулами:

Реакция нейтрализации в терминах теории Льюиса рассматривается как присоединение электронной пары гидроксид-иона к иону водорода, предоставляющему для размещения этой пары свободную орбиталь:

Таким образом, сам протон, легко присоединяющий электронную пару, с точки зрения теории Льюиса, выполняет функцию кислоты. В этой связи, кислоты по Бренстеду могут рассматриваться как продукты реакции между льюисовскими кислотами и основаниями. Так, HCl является продуктом нейтрализации кислоты H + основанием Cl - , а ион H 3 O + образуется в результате нейтрализации кислоты H + основанием H 2 O.
Реакции между кислотами и основаниями Льюиса также иллюстрируют следующие примеры:
К основаниям Льюиса также относят галогенид-ионы, аммиак, алифатические и ароматические амины, кислородсодержащие органические соединения типа R 2 CO, (где R- органический радикал).
К кислотам Льюиса относят галогениды бора, алюминия, кремния, олова и других элементов.
Очевидно, что в теории Льюиса понятие «кислота» включает в себя более широкий круг химических соединений. Это объясняется тем, что по Льюису отнесение вещества к классу кислот обусловлено исключительно строением его молекулы, определяющим электронно-акцепторные свойства, и не обязательно связано с наличием атомов водорода. Льюисовские кислоты, не содержащие атомов водорода, называют апротонными .
РАСТВОРЫ
Общие сведения
Растворы - это гомогенные системы переменного состава, состоящие из двух и более веществ, называемых компонентами. По агрегатному состоянию растворы могут быть газообразными (воздух), жидкими (кровь, лимфа) и твердыми (сплавы). В медицине наибольшее значение имеют жидкие растворы, которые играют исключительную роль в жизнедеятельности живых организмов. С образованием растворов связаны процессы усвоения пищи и выведения из организма продуктов жизнедеятельности. В форме растворов вводится большое количество лекарственных препаратов.
Для качественного и количественного описания жидких растворов используются термины «растворитель» и «растворенное вещество» , хотя в некоторых случаях такое разделение является достаточно условным. Так, медицинский спирт (96% раствор этанола в воде) скорее следует рассматривать как раствор воды в спирте. Все растворители делятся на неорганические и органические. Важнейшим неорганическим растворителем (а в случае биологических систем – единственным) является вода. Это обусловлено такими свойствами воды, как полярность, низкая вязкость, склонность молекул к ассоциации, относительно высокие температуры кипения и плавления. Растворители органической природы разделяют на полярные (спирты, альдегиды, кетоны, кислоты) и неполярные (гексан, бензол, четыреххлористый углерод).
Процесс растворения в равной степени зависит как от природы растворителя, так и от свойств растворенного вещества. Очевидно, что способность образовывать растворы выражена у разных веществ по-разному. Одни вещества могут смешиваться друг с другом в любых количествах (вода и этанол), другие – в ограниченных (вода и фенол). Однако, следует помнить: абсолютно нерастворимых веществ не существует!
Склонность вещества растворяться в том или ином растворителе можно определить, используя простое эмпирическое правило: подобное растворяется в подобном. Действительно, вещества с ионным (соли, щелочи) или полярным (спирты, альдегиды) типом связи хорошо растворимы в полярных растворителях, например, в воде. И наоборот, растворимость кислорода в бензоле на порядок выше чем в воде, так как молекулы O 2 и C 6 H 6 неполярны.
Степень сродства соединения к определенному типу растворителя можно оценить, анализируя природу и количественное соотношение входящих в его состав функциональных групп, среди которых выделяют гидрофильные (притягивающие воду) и гидрофобные (отталкивающие воду). К гидрофильным относят полярные группы, такие как гидроксильная (-OH), карбоксильная (-COOH), тиольная (-SH), амино (-NH 2). Гидрофобными считают неполярные группы: углеводородные радикалы алифатического (-CH 3 , -C 2 H 5) и ароматического (-C 6 H 5) рядов. Соединения, имеющие в своем составе как гидрофильные, так и гидрофобные группы, называют дифильными . К таким соединениям относят аминокислоты, белки, нуклеиновые кислоты.
Теории растворов
В настоящее время известны две основные теории растворов: физическая и химическая.
Физическая теория растворов.
Физическая теория растворов была предложена С. Аррениусом (1883) и Я. Г. Вант-Гоффом (1885). В данной теории растворитель рассматривается как химически инертная среда, в которой равномерно распределены частицы (молекулы, ионы) растворенного вещества. При этом предполагается отсутствие межмолекулярного взаимодействия как между частицами растворенного вещества, так и между молекулами растворителя и частицами растворенного вещества. Однако впоследствии выяснилось, что условиям данной модели удовлетворяет поведение лишь малой группы растворов, которые были названы идеальными . В частности, идеальными растворами можно считать газовые смеси и очень сильно разбавленные растворы неэлектролитов.
В середине XIX века общепринятой считалась физическая теория растворов, одним из авторов которой являлся Вант-Гофф (Голландия). Эта теория рассматривала растворы как механические смеси, без учета взаимодействий между молекулами растворителя и частицами растворенного вещества.
Факты, которые не могла объяснить физическая теория растворов:
1) Тепловые эффекты растворения.
Пример. Растворение – процесс экзотермический; растворение – эндотермический.
2) Изменение (чаще – уменьшение) объема жидкости при растворении. Это явление называется контракция.
Пример. При смешивании 50 мл и 50 мл образуется 98 мл раствора
3) Изменение окраски некоторых веществ при растворении и некоторых растворов при выпаривании.
Примеры. Безводный сульфат меди(II) – белый порошок – при поглощении воды синеет.
Розовый раствор хлорида кобальта(II) при высыхании окраску не изменяет, а при последующем выпаривании – синеет.
1),2),3) - признаки химических реакций.
Д. И. Менделеев считал, что рассмотренные явления, безусловно, указывают на какие-то взаимодействия между растворенным веществом и растворителем. Он последовательно развивал мысль о химическом взаимодействии между частицами растворенного вещества и молекулами растворителя. Учение Менделеева было развито и дополнено русскими учеными И. А. Каблуковым и В. А. Кистяковским. На основе этих представлений произошло объединение физической и химической точки зрения на растворы.
Основные положения современной физико-химической теории растворов сводятся к следующему.
1) Растворитель и растворенное вещество химически взаимодействуют между собой.
2) В результате взаимодействия образуются непрочные соединения, называемые сольватами, а сам процесс называется сольватацией. В частном случае, когда растворителем является вода, эти соединения называются гидратами, а процесс – гидратацией.
Сами растворы, а также большинство гидратов (сольватов), которые образуются при растворении, имеют переменный состав. Этим они отличаются от химических соединений.
Физико-химическая теория растворов позволила объяснить многие непонятные до этого факты:
1) Изменение окраски некоторых веществ при растворении и некоторых растворов при выпаривании.
2) Тепловые эффекты при растворении.
Явление гидратации иногда можно наблюдать, не пользуясь специальными приборами. Например, безводный сульфат меди (II) CuSO 4 – белое вещество. При его растворении в воде образуется голубой раствор. Окраска раствора обусловливается гидратированными ионами меди. Гидратированные частички иногда настолько прочны, что при выделении растворенного вещества из раствора в твердую фазу молекулы воды входят в состав кристаллов. Так, при выпаривании водного раствора сульфата меди в твердую фазу выделяется соль CuSO 4 ∙5H 2 O.
Кристаллические вещества, в состав которых входят молекулы воды, называются кристаллогидратами, а содержащаяся в них вода - кристаллизационной
Аналогично объясняется изменение окраски раствора хлорида кобальта(II) при выпаривании. Гидратированные ионы кобальта в растворе - розового цвета, такой же розовый цвет имеет и кристаллогидрат кобальта (II) CoCl 2 ∙6H 2 O. Но при прокаливании на воздухе кристаллогидрат кобальта теряет кристаллизационную воду и превращается в безводный хлорид кобальта(II) синего цвета.
Образованием кристаллогидратов объясняются и тепловые эффекты при растворении. Тепловой эффект растворения складывается из энергии, затраченной на разрушение кристаллической решетки и отделение частиц растворенного вещества друг от друга, а также энергии, которая выделяется при гидратации.
Какой вклад энергии преобладает, такой тепловой эффект в итоге мы и получаем.
Изменение других термодинамических параметров при растворении.
Так как, в целом, при растворении беспорядок в системе увеличивается.
Так как растворение – процесс самопроизвольный.
Химическая, или сольватная, теория растворов была предложена в 1887 г. Д.И. Менделеевым, который установил, что в реальном растворе присутствуют не только индивидуальные компоненты, но и продукты их взаимодействия. Исследования водных растворов серной кислоты и этилового спирта, проведенные Д.И. Менделеевым, легли в основу теории, суть которой заключается в том, что между частицами растворенного вещества и молекулами растворителя происходят взаимодействия, в результате которых образуются нестойкие соединения переменного состава, называемые сольватами или гидратами , если растворителем является вода. Главную роль в образовании сольватов играют непрочные межмолекулярные силы, в частности, водородная связь.
В этой связи следует принять следующую трактовку понятия «раствор»:
Раствором называется гомогенная система переменного состава, состоящая из двух и более компонентов и продуктов их взаимодействия.
Из данного определения следует, что растворы занимают промежуточное положение между химическими соединениями и смесями. С одной стороны, растворы однородны, что позволяет рассматривать их как химические соединения. С другой стороны, в растворах нет строгого стехиометрического соотношения между компонентами. Кроме того, растворы можно разделить на составные части (например, при упаривании раствора NaCl можно выделить соль в индивидуальном виде).
Основные способы выражения концентрации растворов
Количественный состав раствора чаще всего оценивают при помощи понятия концентрации , под которым понимают содержание растворенного вещества (в определенных единицах) в единице массы (объема) раствора (растворителя). Основными способами выражения концентрации растворов являются следующие:
1. Массовая доля вещества (x ) это отношение массы данного компонента x, содержащегося в системе, к общей массе этой системы:
Единицей количества вещества является моль, т. е. то количество вещества, которое содержит столько реальных или условных частиц, сколько атомов содержится в 0,012 кг изотопа С 12 . При использовании моля как единицы количества вещества следует знать, какие частицы имеются в виду: молекулы, атомы, электроны или другие. Молярная масса М(х) это отношение массы к количеству вещества (г/моль):
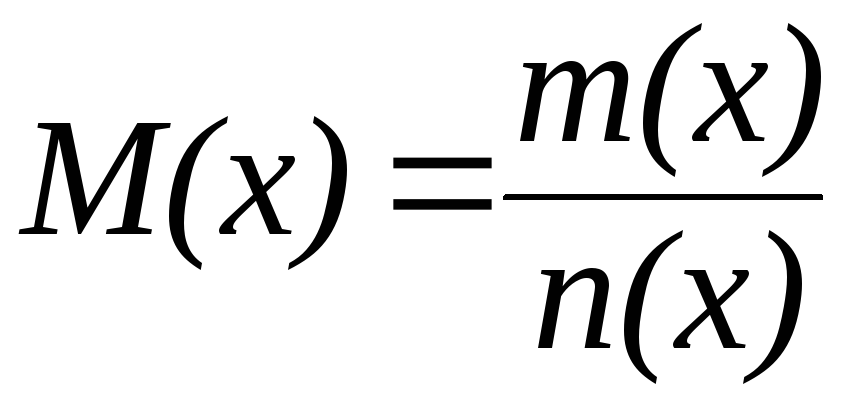
3. Молярная концентрация эквивалента С(x ) это отношение количества эквивалента вещества n(x) к объему раствора V р-ра:
|
|
Химический эквивалент – это реальная или условная частица вещества, которая может замещать, присоединять или высвобождать 1 ион водорода в кислотно-основных или ионообменных реакциях.
Так же, как молекула, атом или ион, эквивалент безразмерен.
Масса моля эквивалентов называется молярной массой эквивалента М(x ). Величина называется фактором эквивалентности . Она показывает, какая доля реальной частицы вещества соответствует эквиваленту. Для правильного определения эквивалента вещества надо исходить из конкретной реакции, в которой это вещество участвует, например, в реакции взаимодействия Н 3 РО 4 с NaOH может происходить замещение одного, двух или трех протонов:
1. H 3 PO 4 + NaOH NaH 2 PO 4 + H 2 O;
2. H 3 PO 4 + 2NaOH Na 2 HPO 4 + 2H 2 O;
3. H 3 PO 4 + 3NaOH Na 3 PO 4 + 3H 2 O.
В
соответствии с определением эквивалента,
в 1-й реакции замещается один протон,
следовательно, молярная масса эквивалента
вещества равна молярной массе, т. е.
z l
и 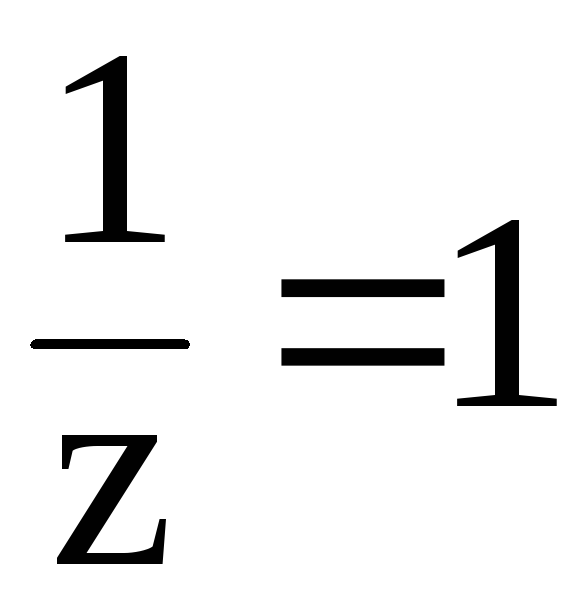 .
В данном случае:
.
В данном случае:
Во 2-й
реакции происходит замещение двух
протонов, следовательно, молярная масса
эквивалента составит половину молярной
массы Н 3 РО 4 ,
т. e.
z 2,
а .
Здесь:
.
Здесь:
В 3-й реакции
происходит замещение трех протонов и
молярная масса эквивалента составит
третью часть молярной массы Н 3 РО 4 ,
т.е. z 3,
a
 .
Соответственно:
.
Соответственно:
В реакциях обмена, где непосредственно не участвуют протоны, эквиваленты могут быть определены косвенным путем, введением вспомогательных реакций, анализ результатов которых позволяет вывести правило, что z для всех реакций равен суммарному заряду обменивающихся ионов в молекуле вещества, участвующего в конкретной химической реакции.
1. AlCl 3 + 3AgNO 3 = Al(NO 3) 3 + 3AgCl.
Для AlCl 3 обменивается 1 ион Al 3+ с зарядом +3, следовательно, z = 13 = 3. Таким образом:
Можно также сказать,
что обмениваются 3 иона хлора с зарядом
1.
Тогда z = 31 = 3
и

Для AgNO 3 z = 11 = 1 (обменивается 1 ион Ag + с зарядом +1 или обменивается 1 ион NO 3 с зарядом 1).
2. Al 2 (SO 4) 3 + 3BaCl 2 = 3BaSO 4 + 2AlCl 3 .
Для Al 2 (SO 4) 3 z = 23 = 6 (обменивается 2 иона Al 3+ с зарядом +3 или 3 иона SO 4 2 с зарядом 2). Следовательно,
Итак,
запись С(H 2 SO 4)
= 0,02 моль/л означает, что имеется раствор,
в 1 л которого содержится 0,02 моль
эквивалента H 2 SO 4 ,
а молярная масса эквивалента H 2 SO 4
составляет при этом
молярной массыH 2 SO 4 ,
т. е. 1 л раствора содержит
 H 2 SO 4 .
H 2 SO 4 .
При
факторе эквивалентности  молярная концентрация эквивалента
равна молярной концентрации раствора.
молярная концентрация эквивалента
равна молярной концентрации раствора.
4. Титр Т(x ) – это отношение массы вещества к объему раствора (в мл):
6. Мольная доля N(x ) – это отношение количества вещества данного компонента,содержащегося всистеме, к общему количеству веществ системы:
|
|
Выражается в долях единицы или в %.
7. Коэффициентом растворимости вещества Р(x ) называют максимальную массу вещества, выраженную в г, которая может раствориться в 100 г растворителя.
Раствор – это однородная смесь переменного состава, состоящая из растворяемого вещества, растворителя и продуктов их взаимодействия.
Раствор, в котором данное вещество при определённой температуре больше не растворяется, называется насыщенным , а раствор, в котором это вещество ещё может растворяться, – ненасыщенным .
Кристаллогидраты
Если растворитель – вода, то продукты присоединения молекул воды к частицам растворяемого вещества называются гидратами , а процесс их образования – гидратацией .
Гидраты – очень неустойчивые соединения, и при выпаривании воды из раствора они легко разрушаются. Однако некоторые гидраты могут удерживать воду даже в твёрдом кристаллическом состоянии.
Такие вещества называют кристаллогидратами . Кристаллогидратами является большинство природных минералов. Много веществ получают в чистом виде в форме кристаллогидратов.
Химическая теория была предложена Д.И. Менделеевым. Согласно представлениям Д.И. Менделеева между молекулами растворяемого вещества и растворителем происходит химическое взаимодействие с образованием неустойчивых, превращающихся друг в друга соединений растворенного вещества с растворителем – сольватов.
Сольваты – это неустойчивые соединения переменного состава. Если растворителем является вода, их называют гидратами . Сольваты (гидраты) образуются за счет ион-дипольного, донорно-акцепторного взаимодействий, образования водородных связей и т.д.
9.Концентрация растворов. Растворимость, насыщенные и ненасыщенные растворы.
Концентрация – это относительное количество растворенного вещества в растворе.
Молярная концентрация (С)– это отношение количества растворенного вещества v (в молях) к объему раствора V в литрах.
Единица молярной концентрации – моль/л. Зная число молей вещества в 1 л раствора, легко отмерить нужное количество молей для реакции с помощью подходящей мерной посуды.
Массовая доля растворенного вещества – это отношение массы растворенного вещества m 1 к общей массе раствора m, выраженное в процентах.
Нормальность раствора обозначает число грамм-эквивалентов данного вещества в одном литре раствора или число миллиграмм-эквивалентов в одном миллилитре раствора. Грамм - эквивалентом вещества называется количество граммов вещества, численно равное его эквиваленту.
Раствори́мость - способность вещества образовывать с другими веществами однородные системы - растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц.
Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах, отнесённых к 100 г или 100 см³ растворителя.
Ненасыщенный раствор - раствор, в котором концентрация растворенного вещества меньше, чем в насыщенном растворе, и в котором при данных условиях можно растворить ещё некоторое его количество.
Насыщенный раствор - раствор, в котором растворённое вещество при данных условиях достигло максимальной концентрации и больше не растворяется. Осадок данного вещества находится в равновесном состоянии с веществом в растворе.


